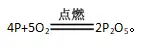
╬³╦«Ę©£yČ©č§ÜŌĄ─║¼┴┐
1Ż«£yČ©įŁ└Ē
└¹ė├╚╝¤²Ę©£yČ©┐šÜŌųąč§ÜŌĄ─║¼┴┐Ą─įŁ└Ē╩Ū└¹ė├╝t┴ū╚╝¤²Ž¹║─├▄ķ]╚▌Ų„ā╚┐šÜŌųąĄ─č§ÜŌ�Ż¼╩╣├▄ķ]╚▌Ų„ā╚ē║ÅŖ£pąĪ��Ż¼į┌┤¾ÜŌē║Ą─ū„ė├Ž┬Ż¼▀M╚ļ╚▌Ų„ā╚╦«Ą─¾wĘe╝┤×ķ£p╔┘Ą─č§ÜŌĄ─¾wĘe��ĪŻĘ┤æ¬Ą─╗»īWĘĮ│╠╩Į
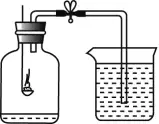
2Ż«īŹ“×čbų├
Ż©1Ż®āxŲ„Ż║╝»ÜŌŲ┐Īó╚╝¤²│ūĪóī¦╣▄Īó¤²▒Ł����ĪóŽ─z╣▄�ĪóÅŚ╗╔ŖA�ĪŻ
Ż©2Ż®╦ÄŲĘŻ║╝t┴ūĪó╦«�ĪŻ
3Ż«īŹ“×▓Į¾E
Ż©1Ż®Ž╚į┌╝»ÜŌŲ┐ā╚╝ė╚ļ╔┘┴┐╦«��Ż¼▓óū÷╔Žėø╠¢ĪŻ
Ż©2Ż®▀BĮėčbų├�ĪŻ
Ż©3Ż®Öz▓ķčbų├Ą─ÜŌ├▄ąį����ĪŻ
Ż©4Ż®ė├ÅŚ╗╔ŖAŖAŠoŽ─z╣▄���ĪŻ
Ż©5Ż®³c╚╝╝t┴ū��Ż¼čĖ╦┘╔ņ╚ļ╝»ÜŌŲ┐ā╚�ĪŻ
Ż©6Ż®╚╝¤²ĮY╩°└õģsų┴╩ę£ž║¾�����Ż¼┤“ķ_ÅŚ╗╔ŖA��ĪŻ
4Ż«īŹ“×¼FŽ¾
ó┘ ╝t┴ū╚╝¤²Ż¼«a╔·┤¾┴┐░ū¤¤(╬Õč§╗»Č■┴ūąĪŅw┴Ż)Ż╗ó┌ Ę┼¤ßŻ╗ó█ └õģs║¾┤“ķ_ÅŚ╗╔ŖA�Ż¼╦«čžų°ī¦╣▄▀M╚ļ╝»ÜŌŲ┐ųą����Ż¼▀M╚ļ╝»ÜŌŲ┐ā╚╦«Ą─¾wĘe╝sš╝╝»ÜŌŲ┐┐šÜŌ┐é¾wĘeĄ─1/5��ĪŻ
5Ż«īŹ“×│╔╣”Ą─ĻPµI
Ż©1Ż®╝t┴ūę¬▀^┴┐ĪŻ
Ż©2Ż®čbų├▒žĒÜ├▄ĘŌ���ĪŻ
Ż©3Ż®ī¦╣▄ā╚Ž╚ūóØM╦«ĪŻ
Ż©4Ż®└õģsĄĮ╩ę£ž║¾����Ż¼┤“ķ_ÅŚ╗╔ŖA�ĪŻ
6Ż«īŹ“×Ęų╬÷┼cĮYšō
╝t┴ū╚╝¤²╔·│╔╬Õč§╗»Č■┴ū╣╠¾w��Ż¼╬Õč§╗»Č■┴ūśOęū╚▄ė┌╦«����Ż¼▓╗š╝ėą¾wĘe���ĪŻ╝t┴ū╚╝¤²Ž¹║─┴╦╝»ÜŌŲ┐ā╚Ą─č§ÜŌ�Ż¼└õģs║¾Ż¼┤¾ÜŌē║░č¤²▒Łā╚Ą─╦«ē║▀M╝»ÜŌŲ┐Ż¼ē║▀MĄ─╦«Ą─¾wĘe╝s╩Ū╝»ÜŌŲ┐ā╚Ž¹║─Ą─č§ÜŌĄ─¾wĘe��Ż¼ė╔┤╦ūC├„┐šÜŌųąč§ÜŌ╝sš╝┐šÜŌ┐é¾wĘeĄ─ 1/5�����ĪŻ
ūóęŌŻ║═©▀^┤╦īŹ“×ę▓─▄Ą├│÷Ą¬ÜŌ▓╗╚╝¤²�����Īó▓╗ų¦│ų╚╝¤²╝░▓╗ęū╚▄ė┌╦«Ą─ąį┘|ĪŻ
7Ż«īŹ“×ūóęŌ╩┬ĒŚ
1. ╝t┴ū▒žĒÜ▀^┴┐����ĪŻ╚ń╣¹╝t┴ūĄ─┴┐▓╗ūŃ�����Ż¼╝»ÜŌŲ┐ā╚Ą─č§ÜŌø]ėą▒╗═Ļ╚½Ž¹║─���Ż¼£y┴┐ĮY╣¹Ģ■Ų½ąĪ�����ĪŻ
2. čbų├ÜŌ├▄ąįę¬║├�ĪŻ╚ń╣¹čbų├Ą─ÜŌ├▄ąį▓╗║├�Ż¼╝»ÜŌŲ┐═ŌĄ─┐šÜŌ▀M╚ļ╝»ÜŌŲ┐Ż¼£y┴┐ĮY╣¹Ģ■Ų½ąĪ��ĪŻ
3. ī¦╣▄ųąę¬ūóØM╦«ĪŻĘ±ät«ö╝t┴ū╚╝¤²▓ó└õģs║¾����Ż¼▀M╚ļĄ─╦«Ģ■ėąę╗▓┐ĘųÜł┴¶į┌įć╣▄ųą��Ż¼ī¦ų┬£y┴┐ĮY╣¹Ų½ąĪĪŻ
4. └õģs║¾į┘┤“ķ_ÅŚ╗╔ŖA����Ż¼Ę±ät£y┴┐ĮY╣¹Ų½ąĪ��ĪŻ
5. ╚ń╣¹ÅŚ╗╔ŖA╬┤ŖAŠoŻ¼╗“š▀╚¹╚¹ūėĄ─äėū„╠½┬²��Ż¼£y┴┐ĮY╣¹Ģ■Ų½┤¾�����ĪŻ
6. į┌╝»ÜŌŲ┐Ąū╝ė╦«Ą──┐Ą─Ż║╬³╩šėąČŠĄ─╬Õč§╗»Č■┴ū���ĪŻ
7. ▓╗ę¬ė├─Š╠┐╗“┴“┤·╠µ╝t┴ū���ŻĪįŁę“Ż║─Š╠┐║═┴“╚╝¤²▒M╣▄Ž¹║─ÜŌ¾w���Ż¼Ą½╩Ū«a╔·┴╦ą┬Ą─ÜŌ¾wŻ¼ÜŌ¾w¾wĘe▓╗ūā���Ż¼╚▌Ų„ā╚ē║ÅŖÄū║§▓╗ūāŻ¼╦«├µ▓╗Ģ■ėąūā╗»����ĪŻČ°╝ÜĶFĮzį┌┐šÜŌųąļyęį╚╝¤²���Ż¼č§ÜŌĄ─¾wĘeÄū║§▓╗Ģ■ūā╗»����Ż¼ę“┤╦├▄ķ]╚▌Ų„ā╚╦«├µ▓╗╔Ž╔²���ĪŻ
8. ╚ń╣¹ŅAŽ╚į┌╝»ÜŌŲ┐ā╚Ę┼╚ļÜõč§╗»Ōc╚▄ę║����Ż¼Š═┐╔ęįė├─Š╠┐╗“┴“┤·╠µ╝t┴ū▀MąąīŹ“×ĪŻ
9. ▓╗ę¬ė├µV┤·╠µ╝t┴ū�����ŻĪįŁę“Ż║µVį┌┐šÜŌųą╚╝¤²Ģr─▄┼cĄ¬ÜŌ║═Č■č§╗»╠╝░l╔·Ę┤æ¬�Ż¼▀@śė▓╗āHŽ¹║─č§ÜŌŻ¼▀ĆŽ¹║─┴╦Ą¬ÜŌ║═Č■č§╗»╠╝Ż¼╩╣£y┴┐ĮY╣¹Ų½┤¾��ĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖC���ĪóŲĮ░ÕĄ╚ęŲäėįOéõįLå¢ųą┐╝ŠW�����Ż¼2024ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąą�ŻĪ>>³cō¶▓ķ┐┤











