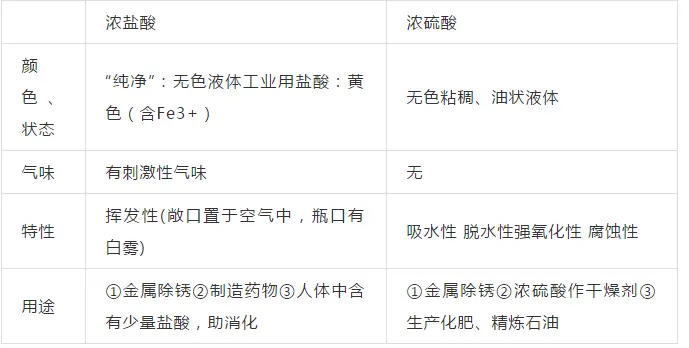
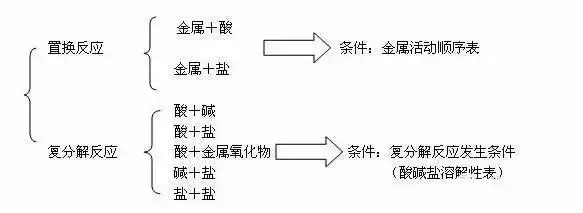
ę╗�����Īó╦ß�ĪóēA���Īó¹}Ą─ĮM│╔
╦ß╩Ūė╔Üõį¬╦ž║═╦ßĖ∙ĮM│╔Ą─╗»║Ž╬’ ╚ńŻ║┴“╦ß(H2SO4)�Īó¹}╦ß(HCl)ĪóŽ§╦ß(HNO3)
ēA╩Ūė╔Įī┘į¬╦ž║═Üõč§Ė∙ĮM│╔Ą─╗»║Ž╬’ ╚ńŻ║Üõč§╗»Ōc��ĪóÜõč§╗»Ō}���Īó░▒╦«(NH3·H2O)
¹}╩Ūė╔Įī┘į¬╦žį¬╦ž(╗“õ@Ė∙)║═╦ßĖ∙ĮM│╔Ą─╗»║Ž╬’ ╚ńŻ║┬╚╗»Ōc�Īó╠╝╦ßŌc
╦ßĪóēA���Īó¹}Ą─╦«╚▄ę║┐╔ęįī¦ļŖ(įŁę“Ż║╚▄ė┌╦«ĢrļxĮŌą╬│╔ūįė╔ęŲäėĄ─ĻÄ����ĪóĻ¢ļxūė)
Č■Īó╦ß
1��ĪóØŌ¹}╦ß��ĪóØŌ┴“╦ߥ─╬’└Ēąį┘|�����Īó╠žąįĪóė├═Š
2����Īó╦ߥ─═©ąį(Š▀ėą═©ąįĄ─įŁę“Ż║╦ßļxĮŌĢr╦∙╔·│╔Ą─Ļ¢ļxūė╚½▓┐╩ŪH+)
(1)┼c╦ßēAųĖ╩Šä®Ą─Ę┤æ¬Ż║╩╣ūŽ╔½╩»╚’įćę║ūā╝t╔½�Ż¼▓╗─▄╩╣¤o╔½Ęė╠¬įćę║ūā╔½
(2)Įī┘ + ╦ß → ¹} + ÜõÜŌ
(3)ēAąįč§╗»╬’ + ╦ß → ¹} + ╦«
(4)ēA + ╦ß → ¹} + ╦«
(5)¹} + ╦ß → ┴Ēę╗ĘN¹} + ┴Ēę╗ĘN╦ß(«a╬’Ę¹║ŽÅ═ĘųĮŌŚl╝■)
3���Īó╚²ĘNļxūėĄ─Öz“×

╚²�����ĪóēA
1��ĪóÜõč§╗»ŌcĪóÜõč§╗»Ō}Ą─╬’└Ēąį┘|Īóė├═Š

2�ĪóēAĄ─═©ąį(Š▀ėą═©ąįĄ─įŁę“Ż║ļxĮŌĢr╦∙╔·│╔Ą─ĻÄļxūė╚½▓┐╩ŪOH-)
(1)ēA╚▄ę║┼c╦ßēAųĖ╩Šä®Ą─Ę┤æ¬Ż║╩╣ūŽ╔½╩»╚’įćę║ūā╦{╔½���Ż¼╩╣¤o╔½Ęė╠¬įćę║ūā╝t╔½
(2)╦ßąįč§╗»╬’+ēA → ¹}+╦«
(3)╦ß+ēA → ¹}+╦«
(4)¹}+ēA → ┴Ēę╗ĘN¹}+┴Ēę╗ĘNēA(Ę┤æ¬╬’Š∙┐╔╚▄����Ż¼«a╬’Ę¹║ŽÅ═ĘųĮŌŚl╝■)
ūóŻ║
ó┘ļy╚▄ąįēA╩▄¤ßęūĘųĮŌ(▓╗ī┘ė┌ēAĄ─═©ąį)
╚ńCu(OH)2 ΔCuO +H2O
2Fe(OH)3 ΔFe2O3+3H2O
ó┌│ŻęŖ│┴ĄĒŻ║AgCl↓ BaSO4↓ Cu(OH)2↓ F e(OH)3↓ Mg(OH)2↓ BaCO3↓ CaCO3↓
ó█Å═ĘųĮŌĘ┤æ¬Ą─Śl╝■Ż║«öā╔ĘN╗»║Ž╬’╗źŽÓĮ╗ōQ│╔Ęų��Ż¼╔·│╔╬’ųąėą│┴ĄĒ╗“ėąÜŌ¾w╗“ėą╦«╔·│╔Ģr���Ż¼Å═ĘųĮŌĘ┤æ¬▓┼┐╔ęį░l╔·ĪŻ
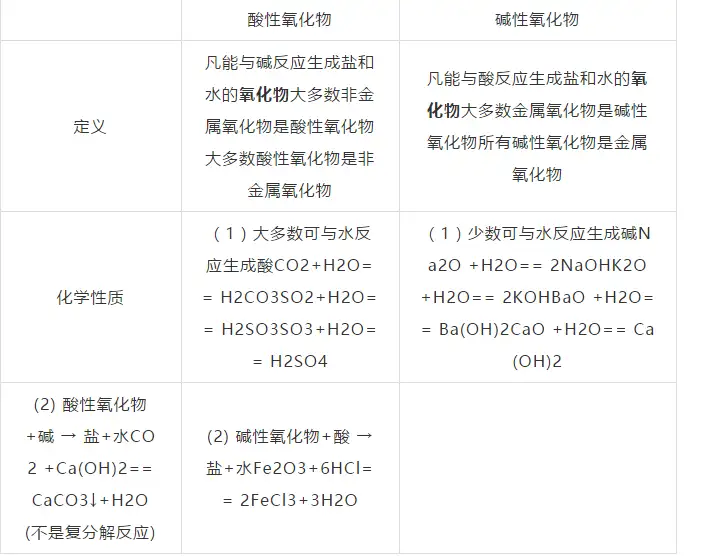
╦─�����Īó╦ßąįč§╗»╬’┼cēAąįč§╗»╬’
╬Õ��Īóųą║═Ę┤æ¬ ╚▄ę║╦ßēAČ╚Ą─▒Ē╩ŠĘ©--pH
1�����ĪóČ©┴xŻ║╦ß┼cēAū„ė├╔·│╔¹}║═╦«Ą─Ę┤æ¬
2Īóæ¬ė├Ż║
(1)Ė─ūā═┴╚└Ą─╦ßēAąį
(2)╠Ä└Ē╣żÅSĄ─ÅU╦«
(3)ė├ė┌ßt╦Ä
3�����Īó╚▄ę║╦ßēAČ╚Ą─▒Ē╩ŠĘ©--pH
(1)
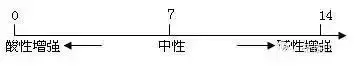
(2)pHĄ─£yČ©Ż║ūŅ║åå╬Ą─ĘĮĘ©╩Ū╩╣ė├pHįć╝ł
ė├▓Ż┴¦░¶(╗“Ą╬╣▄)š║╚Ī┤²£yįćę║╔┘įS�Ż¼Ą╬į┌pHįć╝ł╔ŽŻ¼’@╔½║¾┼cś╦£╩▒╚╔½┐©ī”šš����Ż¼ūx│÷╚▄ę║Ą─pH(ūxöĄ×ķš¹öĄ)
(3)╦ßėĻŻ║š²│ŻėĻ╦«Ą─pH╝s×ķ5.6(ę“×ķ╚▄ėąCO2)
pH<5.6Ą─ėĻ╦«×ķ╦ßėĻ

╦ßēA¹}ąį┘|ų«╦ߥ─═©ąį
╦ߥ─ĮM│╔——Üõļxūė+╦ßĖ∙ļxūė
(1)Ė·ųĖ╩Šä®Ę┤æ¬
ūŽ╔½╩»╚’įćę║ė÷╦ßūā╝t╔½
¤o╔½Ęė╠¬įćę║ė÷╦ß▓╗ūā╔½
(2)╦ߥ─PH<7
(3)Ė·(H)Ū░Ą─╗ŅØŖĮī┘Ųų├ōQĘ┤æ¬
╦ß + Įī┘==¹} + ÜõÜŌ
└²Ż║2HCl+Fe=FeCl2+H2↑
(4) Ė·ēAąįč§╗»╬’║═─│ą®Įī┘č§╗»╬’Ę┤æ¬
╦ß + ēAąį(Įī┘)č§╗»╬’—→¹}+╦«
└²Ż║3H2SO4+Fe2O3=Fe2(SO4)3+3H2O
(5)Ė·─│ą®¹}Ę┤æ¬
╦ß+╠╝╦ß¹}==¹}+╦«
╦ß+¹}—→ą┬╦ß+ą┬¹}
└²Ż║H2SO4+BaCl2=2HCl+BaSO4↓
(6)Ė·ēAŲųą║═Ę┤æ¬
╦ß+ēA—→¹}+╦«
└²Ż║2HCl+Cu(OH)2=CuCl2+2H2O

│§ųą╗»īW╦ßēA¹}
Ą─Å═┴Ģ╝░ųž³cŅ}ą═ĮŌ╬÷
į┌Ė„╩Ī╩ąųą┐╝įćŠĒĄ─├³Ņ}ųą�Ż¼¤o▓╗īó╦ßēA¹}Ą─╗»īWąį┘|Ą─┐╝▓ņū„×ķųžųąų«ųžĪŻŲõŅ}ą═ų«ČÓūā╗»ų«┤¾�����Ż¼ī”ė┌═¼īWéāüĒųv┤_ėąŪ¦Ņ^╚fŠw�����Īó┴”▓╗Å─ą─ų«Ėą�Ī����Ż╗∙ė┌┤╦��Ż¼╣Pš▀ĮY║ŽĮ╠īWīŹ█`£\šäę╗Ž┬ėąĻP╦ßēA¹}Ą─Å═┴Ģ�����Ż¼ęįŲ┌ī”═¼īWéāĄ─Å═┴Ģėą╦∙ų·ęµĪŻ
ę╗�Īó╩ņŠÜėøæøęÄ┬╔╩Ūæ¬ė├Ą─Ū░╠ß
╦ßēA¹}▓┐Ęųļm╚╗Ņ}ą═▒ŖČÓ�����Ż¼╚ńŻ║ĶbäeĪó═ŲöÓ�����Īó│²ļs……����Ż¼Ą½╩Ū▀@ą®æ¬ė├ļx▓╗ķ_ūŅ╗∙ĄAĄ─ų¬ūR³cŻ║╝┤Ż║ī”╦ßēA¹}╗»īWąį┘|Ą─╩ņŠÜėøæøĪŻ
═©▀^īW┴Ģ┐╔ų¬Ż║╦ߥ─═©ąįėą╬Õ³c���ĪóēA║═¹}Ą─═©ąįĖ„ėą╦─³cĪŻī”ė┌▀@ą®╗»īWąį┘|▒žĒÜ╝ėęįÅŖ╗»ėøæø║═ņ`╗Ņėøæø����Ī�Ż┐╔▓╔ė├łD▒ĒėøæøĘ©ęį╝░ūā╩ĮėøæøĘ©Ą╚�����ĪŻ
╚ńŻ║īó╦ßēA¹}Ą─╗»īWąį┘|ØŌ┐s×ķŽ┬łDėøæø▌^║├(łD▒ĒėøæøĘ©)
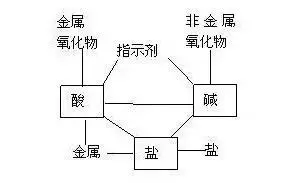
į┌┤╦╗∙ĄA╔Ž����Ż¼į┘ū÷ūā╩ĮŠÜ┴Ģ����Ż¼į÷╝ėī”╗»īWąį┘|Ą─ČÓĮŪČ╚ėøæø(ūā╩ĮėøæøĘ©)����ĪŻ╚ńŻ║
(1)╔·│╔¹}║═╦«Ą─ęÄ┬╔Ż¼ę╗Č©╩Ūųą║═Ę┤æ¬åß?
(2)į┌╦ßēA¹}Ą─╗»īWąį┘|ųąŻ¼╔·│╔¹}Ą─ęÄ┬╔ėąÄūŚlĄ╚�ĪŻ
═©▀^╚ń╔ŽŠÜ┴Ģ���Ż¼╝┤┐╔ŲĄĮ╝ėÅŖų¬ūRĄ─═¼╗»║═«É╗»Ą─ū„ė├�����ĪŻ
Č■ĪóšŲ╬š“ęÄŠž”Ż¼┐╔│╔“ĘĮłA”
ėøæøūĪęį╔ŽęÄ┬╔Š═┐╔ęį╩ņŠÜæ¬ė├┴╦åß?«ö╚╗▓╗─▄ĪŻį┌┤¾┴┐ŠÜ┴Ģųą═¼īWéā░l¼Fęį╔ŽęÄ┬╔ųąėą║▄ČÓ╩Ūėą “ęÄŠž” ėąŚl╝■Ą─��ĪŻę“┤╦į┌ėøūĪęÄ┬╔Ą─Ū░╠ߎ┬�Ż¼▀Ćę¬ėøūĪęÄ┬╔æ¬ė├Ą─Śl╝■Ż¼▀@śė▓┼─▄ū÷ĄĮėąĄ─Ę┼╩ĖĄ─æ¬ė├ĪŻ▒╚╚ńŻ║┐╔Ė∙ō■▓╗═¼Ę┤æ¬ŅÉą═üĒņ`╗ŅėøæøėąĻPĘ┤æ¬Ą─Śl╝■�ĪŻÜw╝{╚ńŽ┬Ż║
└²╚ńŻ║īæ│÷Ž┬┴ą╬’┘|ųąā╔ā╔ų«ķg─▄░l╔·Ę┤æ¬Ą─╗»īWĘĮ│╠╩Į�����ĪŻ
ĶFĪóč§╗»ĶF��Īó¤²ēA╚▄ę║�����ĪóŽĪ┴“╦ß�Īó┴“╦ßŃ~╚▄ę║Īó┬╚╗»õ^╚▄ę║ĪóČ■č§╗»╠╝
╦╝┬Ę³cō▄Ż║
┤╦ŅÉŅ}─┐╩Ū┐╝▓ņ╦ßĪóēAĪó¹}�Īóč§╗»╬’ų«ķgĘ┤æ¬ęÄ┬╔║═Ę┤æ¬░l╔·Śl╝■Ą─▌^║├ĘČ└²����ĪŻĮŌŅ}Ģr���Ż¼×ķĘ└ų╣«a╔·üG┬õ¼FŽ¾����Ż¼┐╔▓╔ė├ęįĶF×ķŲ³cų┤╬Ž“║¾čė╔ņ┼ąöÓĘ┤æ¬╩Ūʱ░l╔·�Ż¼į┘ęįč§╗»ĶF×ķą┬Ų³cų┤╬Ēś═Ų……Ą─ĘĮĘ©ĪŻĮø┼ąöÓ╣▓░l╔·8éĆĘ┤æ¬ĪŻė╔ęį╔Ž┐╔ęį┐┤│÷Ż║į┌┼ąöÓĄ─▀^│╠ųą����Ż¼ūį╚╗ÅŖ╗»┴╦ėąĻPĘ┤æ¬ęÄ┬╔ęį╝░Ę┤æ¬░l╔·Śl╝■Ą─ėøæø�ĪŻ▀@śėĄ─┴ĢŅ}═¼īWéā┐╔ČÓšęę╗ą®��Ż¼ū÷│╔┐©Ų¼│Żéõū¾ėę�Ż¼ļSĢr╝ėęįŠÜ┴Ģ��Ż¼╣”ĄĮūį╚╗│╔�ĪŻ
╚²�����Īóūźųž³cŅ}ą═�Ż¼īWĢ■ęį³cĦ├µ
į┌Å═┴ĢųąĮø│ŻęŖĄĮ▓╗╔┘═¼īW┬±Ņ^ė┌Ņ}║Żų«ųą����Ż¼║─ĢrķL╩šą¦╔§╬óĪŻ╦ßēA¹}▓┐ĘųĄ─Ņ}ą═ļmą╬╩ĮČÓśė�����Ż¼Ą½╚fūā▓╗ļxŲõū┌�ĪŻŠC║Žų«Ž┬Ż¼┐╔ęįšfĶbäeĪó│²ļs�Īó═ŲöÓ▀@╚²ŅÉŅ}ą═╩Ū║▄Š▀┤·▒ĒąįĄ─�Ż¼╦³éāĄ─š²┤_└ĒĮŌ║═šŲ╬š���Ż¼ī”ė┌╠ßĖ▀Ųõ╦¹ŽÓĻPŅ}ą═Ą─æ¬ūā─▄┴”����Ż¼▒žīóŲĄĮ║▄║├Ą─▌Ś╔õū„ė├����ĪŻŽ┬├µĮY║ŽŽÓĻP└²Ņ}║åę¬Üw╝{ę╗Ž┬Ė„ūį╠ž³cĪŻ
└²ę╗Ż║Ęųäe▀xė├ę╗ĘNįćä®ĶbäeęįŽ┬Ė„ĮM╚▄ę║Ż║
A NaOH����ĪóNaCl╚▄ę║��ĪóŽĪHCl ()
B Na2CO3ĪóAgNO3╚▄ę║���ĪóKNO3╚▄ę║ ()
C K2CO3ĪóBaCl2╚▄ę║����ĪóNaCl╚▄ę║ ( )
D NaOH��ĪóCa(OH)2╚▄ę║ĪóŽĪHCl ( )
E NH4NO3�Īó(NH4)2SO4��ĪóNa2CO3ĪóNaCl╚▄ę║ ( )
╦╝┬Ę³cō▄Ż║
ĶbäeŅ}Ą─įŁät╩ŪŻ║ūźūĪ▓╗═¼╬’┘|Ą─ų„ę¬╠žš„�����Ż¼ė├ūŅ║åå╬Ą─ĘĮĘ©�����Ż¼ūŅ╔┘Ą─įćä®�����Ż¼ęįūŅ├„’@Ą─¼FŽ¾Ż¼▀_ĄĮĶbäeĄ──┐Ą─����ĪŻ╦∙ų^ūŅ║åå╬Ą─ĘĮĘ©╩ŪųĖ─▄ė├╬’└ĒĘĮĘ©ĶbäeĄ─Š═▓╗ę¬ė├╗»īWĘĮĘ©Ķbäe;─▄ę╗┤╬ĶbäeĄ─Š═▓╗ė├ČÓ┤╬Ķbäe����ĪŻ╦∙ų^ūŅ╔┘įćä®����Ż¼Š═╩Ū─▄ė├ę╗ĘNįćä®Ķbäeķ_üĒĄ─Š═▓╗ę¬ė├ČÓĘNįćä®ĪŻ╦∙ų^ūŅ├„’@Ą─¼FŽ¾���Ż¼Š═╩Ū═©▀^īŹ“×╩╣Ė„Ķbäe╬’┘|ėą├„’@▓╗═¼Ą─¼FŽ¾ĪŻ╚ńŻ║«a╔·ūā╔½��ĪóĘ┼│÷ÜŌ¾w���Īó╔·│╔│┴ĄĒĄ╚����ĪŻ
ĮŌ╬÷Ż║
AĪó═©▀^╬’┘|ĘųŅÉŻ¼’@╚╗ę└┤╬Ę¹║ŽēAąįĪóųąąįĪó╦ßąį����Ż¼«ö╚╗╝ė╩»╚’įćę║Ķbäe�ĪŻ
B����Īó ═©▀^ė^▓ņ░l¼FŻ║Na2CO3ė÷╦ß(H+)«a╔·ÜŌ¾wŻ¼Č°AgNO3ė÷CL-«a╔·│┴ĄĒ���Ż¼Č°KNO3ė÷¹}╦ߤo¼FŽ¾Ż¼╣╩╝ė¹}╦ßüĒĶbäe����ĪŻ
CĪóė╔╔Ž┐╔ų¬Ż║K2CO3ė÷╦ß(H+)«a╔·ÜŌ¾wŻ¼BaCl2╚▄ę║ė÷SO42-ėą│┴ĄĒŻ¼Č°NaCl╚▄ę║ė÷ŽĪ┴“╦ߤo¼FŽ¾Ż¼╣╩╝ėŽĪ┴“╦ßüĒĶbäeĪŻ
D����ĪóCa(OH)2╚▄ę║ė÷CO32-ėą│┴ĄĒ�Ż¼ŽĪHCl ė÷CO32-ėąÜŌ¾w�Ż¼Č°NaOH ė÷CO32-¤o├„’@¼FŽ¾Ż¼╣╩╝ėNa2CO3╗“K2CO3ĶbäeĪŻ
E�����Īóė^▓ņ┐╔ų¬Ż║NH4+ė÷OH-«a╔·░▒ÜŌ����Ż¼Č°Ba2+ė÷CO32-ĪóSO42-Š∙ėą│┴ĄĒ«a╔·��Ż¼╚Īśė║¾ĘųäeĄ╬╝ėBa(OH)2╚▄ę║����Ż¼ų╗ėąÜŌ¾w«a╔·Ą─╩ŪNH4NO3Ż¼═¼ĢrėąÜŌ¾w║═│┴ĄĒ«a╔·Ą─╩Ū(NH4)2SO4Ż¼ų╗ėą│┴ĄĒ«a╔·Ą─╩ŪNa2CO3����Ż¼¤o¼FŽ¾Ą─╩ŪNaCl�ĪŻ
į┌īŹļHæ¬ė├ųą����Ż¼═¼īWéā▀Ć┐╔ęįīóĶbäeŅ}░┤ę╗┤╬ąįĶbäeĪóČÓ┤╬ąįĶbäeĪó▓╗╝ėŲõ╦¹įćä®Ķbäe��Īóā╔ā╔╗ņ║ŽĶbäeĄ╚▀MąąĘųŅÉ�����Ż¼Ė∙ō■Ė„ūį¬ÜėąĄ─╠ž³cŻ¼┐éĮYĮŌŅ}╝╝Ū╔�����Ż¼Å─Č°▀_ĄĮ╚½├µšŲ╬š▓╗═¼ĶbäeŅÉą═Ą──┐Ą─ĪŻ
└²Č■Ż║▀xė├║Ž▀mĄ─ĘĮĘ©│²╚źŽ┬┴ą╬’┘|ųąĄ─╔┘┴┐ļs┘|
(1)│²╚ź╔·╩»╗ęųąĄ─╠╝╦ßŌ}
(2)│²╚ź┬╚╗»ŌøŠ¦¾wųąĄ─╠╝╦ßŌø
(3)│²╚ź╠╝╦ßŌ}╣╠¾wųąĄ─╠╝╦ßŌc
(4)│²╚źę╗č§╗»╠╝ųąĄ─Č■č§╗»╠╝
(5)│²╚ź┬╚╗»Ōc╚▄ę║ųąĄ─┴“╦ßŃ~
(6)│²╚źCuĘ█ųąĄ─FeĘ█
╦╝┬Ę³cō▄Ż║
│²ļsĄ─įŁät╩ŪŻ║▓╗į÷(▓╗į÷╝ėą┬ļs┘|)��Īó▓╗£p(▓╗£p╔┘įŁ╬’┘|Ą─┴┐)��Īó▓╗ūā(▓╗Ė─ūāįŁ╬’┘|ĀŅæB)�����ĪóęūĘų(│²ļs║¾ęūė┌Ęųļx)ĪóŽ╚╬’║¾╗»(╬’└ĒĘĮĘ©ā׎╚���Ż¼Ųõ┤╬╗»īWĘĮĘ©)ĪŻæ¬ė├ųąėą▐D╗»Ę©��Īó│┴ĄĒĘ©�����Īó╬³╩šĘ©����Īó▀^×VĘ©��Īó╚▄ĮŌĘ©Ą╚ČÓĘN│²ļsĘĮĘ©��ĪŻ
ĮŌ╬÷Ż║
(1)═©▀^Ė▀£ž╝ė¤ß╗“ūŲ¤²Ą─ĘĮĘ©Ż¼╝╚─▄│²╚ź╠╝╦ßŌ}���Ż¼ėų─▄Ą├ĄĮĖ³ČÓ╔·╩»╗ęĪŻ
(2)┐╔╝ė╚ļ▀m┴┐ŽĪ¹}╦ß│õĘųĘ┤æ¬║¾����Ż¼į┘š¶░lĪŻ
(3)┐╔▓╔ė├Ž╚╝ė▀m┴┐╦«╚▄ĮŌ�����Ż¼į┘▀^×VĄ─ĘĮĘ©ĪŻ
(4)┐╔▓╔ė├═©▀^¤ļ¤ßĄ─╠╝īė╗“═©▀^¤²ēA╚▄ę║Ą─ĘĮĘ©����ĪŻĄ½’@╚╗═©▀^¤²ēA╚▄ę║Ą─ĘĮĘ©Š▀ėą╬³╩šļs┘|ÅžĄū��Īó▓┘ū„║åå╬┐ņĮ▌Ą╚ā׳cĪŻ
(5)ė╔ė┌║¼ėąCu2+��ĪóSO42-ā╔ĘNļs┘|ļxūė�Ż¼╣╩┐╔▓╔ė├═¼Ģr│┴ĄĒĘ©ĪŻ╝ė╚ļ▀m┴┐Üõč§╗»õ^╚▄ę║║¾����Ż¼▀^×V╝┤┐╔Ą├┬╚╗»Ōc╚▄ę║��ĪŻ
(6)ė╔ė┌FeĪóCuĘųäe┼┼į┌Įī┘╗ŅäėĒśą“▒ĒųąHĄ─Ū░║¾�����Ż¼╦∙ęį┐╔▓╔ė├╝ė╚ļūŃ┴┐ŽĪ¹}╦ß╗“ŽĪ┴“╦ß╚▄ĮŌ▓ó▀^×VĄ─ĘĮĘ©üĒīŹ¼F��ĪŻę▓┐╔▓╔ė├╝ėūŃ┴┐┴“╦ßŃ~╚▄ę║▓ó▀^×VĄ─ĘĮĘ©�����ĪŻ
└²╚²Īóėąę╗╣╠¾w╗ņ║Ž╬’�����Ż¼┐╔─▄║¼ėąK2CO3�����ĪóK2SO4ĪóCuSO4ĪóCaCl2ĪóKNO3Ą╚╬’┘|ųąĄ─ę╗ĘN╗“ÄūĘN��Ż¼īó╗ņ║Ž╬’╚▄ė┌╦«���Ż¼Ą├¤o╔½╚▄ę║�Ż¼«öĄ╬╚ļŽ§╦ßõ^╚▄ę║Ģr���Ż¼ėą░ū╔½│┴ĄĒ«a╔·�Ż¼į┘╝ėūŃ┴┐Ą─ŽĪŽ§╦ß│┴ĄĒ▓┐Ęų╚▄ĮŌ�Ż¼ätįō╗ņ║Ž╬’ųąę╗Č©║¼ėą____________ę╗Č©▓╗║¼ėą_______________┐╔─▄║¼ėą_____________.
╦╝┬Ę³cō▄Ż║
═ŲöÓŅ}╦∙ė├ĄĮĄ─ų¬ūRā”éõėą╚ńŽ┬Äū³cŻ║(1)╬’┘|Ą─╠ž╩Ō╔½æBĪó╚▄ĮŌąį(░³└©╬’┘|į┌╦«╗“╦ßųąĄ─╚▄ĮŌąį)�ĪŻ╚ńŻ║Ń~ļxūė╚▄ę║×ķ╦{╔½����Ż¼ĶFļxūė╚▄ę║×ķ³S╔½Ą╚�Ż¼│ŻęŖ░ū╔½│┴ĄĒėą╠╝╦ßŌ}Īó╠╝╦ßõ^��Īó╠╝╦ßŃyĪó┬╚╗»Ńy�����Īó┴“╦ßõ^ĪóÜõč§╗»µVĄ╚�ĪŻ╦{╔½│┴ĄĒėąÜõč§╗»Ń~Ż¼╝t║ų╔½│┴ĄĒėąÜõč§╗»ĶF�ĪŻ│§ųą▓╗╚▄ė┌╦ߥ─│┴ĄĒėą┬╚╗»ŃyĪó┴“╦ßõ^����ĪŻ(2)Ģ■┼ąöÓ╬’┘|ų«ķg─▄ʱ░l╔·Ę┤æ¬���ĪŻ(3)╚²ĘNļxūė(┴“╦ßĖ∙�Īó╠╝╦ßĖ∙���Īó┬╚ļxūė)ĶbČ©Ą─š²─µ═Ų└Ē�ĪŻ(4)ī”ė┌ųž³cį~šZĄ─└ĒĮŌ─▄┴”�����ĪŻ╚ńŻ║“╚½▓┐╚▄”�Īó“▓┐Ęų╚▄”���Īó“╚½▓╗╚▄”Ą╚į~Ą─└ĒĮŌ����ĪŻę╗Ą└║├Ą─═ŲöÓŅ}š²╩Ūī”ė┌ęį╔Žų¬ūR³cšŲ╬š│╠Č╚Ą─ŠC║Žąį┐╝▓ņĪŻ
ĮŌ╬÷Ż║═ŲöÓŅ}Ą─ĮŌ┤ę└ō■╩Ū╬’┘|Ą─╠žš„Ę┤æ¬║═Ąõą═Ą─īŹ“×¼FŽ¾ĪŻ┤╦Ņ}ė╔╚▄ė┌╦«Ą├ĄĮ“¤o╔½╚▄ę║”┐╔ų¬Ż║CuSO4(╦{╔½╚▄ę║)ę╗Č©▓╗┤µį┌;═¼ĢrK2CO3�����ĪóCaCl2ė╔ė┌ŽÓė÷Ģ■«a╔·│┴ĄĒ��Ż¼╦∙ęįK2CO3��ĪóCaCl2╗“┤µŲõę╗╗“Š∙▓╗┤µį┌���ĪŻė╔“Ą╬╝ėŽ§╦ßõ^╚▄ę║Ģr��Ż¼ėą░ū╔½│┴ĄĒ«a╔·”┐╔ų¬Ż║│┴ĄĒėą┐╔─▄üĒūįŽ§╦ßõ^┼cK2CO3╗“K2SO4Ę┤æ¬╔·│╔Ą─╠╝╦ßõ^Īó┴“╦ßõ^│┴ĄĒųąĄ─ę╗š▀╗“ā╔š▀��ĪŻė╔“╝ėūŃ┴┐Ą─ŽĪŽ§╦ß│┴ĄĒ▓┐Ęų╚▄ĮŌ”┐╔ų¬Ż║╠╝╦ßõ^�����Īó┴“╦ßõ^Š∙┤µį┌Ż¼▀MČ°═Ų│÷K2CO3��ĪóK2SO4Š∙┤µį┌�����ĪŻę“×ķK2CO3┤µį┌��Ż¼╦∙ęįCaCl2ę╗Č©▓╗┤µį┌ĪŻČ°KNO3ė╔ė┌┤µį┌┼cʱ�Ż¼Š∙▓╗Ģ■ī”ęį╔ŽĶbäe═ŲöÓįņ│╔ė░Ēæ��Ż¼╦∙ęįKNO3┐╔─▄┤µį┌�Ż¼ę▓┐╔ęįšf┐╔─▄▓╗┤µį┌����ĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖCĪóŲĮ░ÕĄ╚ęŲäėįOéõįLå¢ųą┐╝ŠW�����Ż¼2023ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąą��ŻĪ>>³cō¶▓ķ┐┤

















