╚▄ę║ų¬ūR╩Ū│§ųą╗»īWĄ─ę╗éĆųž³c║═ļy³cų¬ūRŻ¼Ųõų„ę¬ųž���Īóļy³cų¬ūRę¬³c░³└©Ż║
(1)’¢║═╚▄ę║║═▓╗’¢║═╚▄ę║Ą─ŽÓ╗ź▐D╗»
(2)╚▄ĮŌČ╚Ą─Ė┼─Ņ╝░Ųõėŗ╦Ń
(3)▀^×V║═ĮYŠ¦ų¬ūRĄ─└ĒĮŌ║═æ¬ė├
(4)╚▄ę║ĮM│╔Ą─▒Ē╩ŠĘĮĘ©╝░Ųõæ¬ė├�����ĪŻ

į┌ę╗ą®┤¾ą═┐╝įć║═Ėé┘ÉįćŅ}ųąŻ¼ĻPė┌╚▄ę║ų¬ūRĄ─įćŅ}═∙═∙╩╣▒ŖČÓ┐╝╔·ĖąĄĮ└¦╗¾║═▌^×ķ╝¼╩ų��ĪŻ×ķ┤╦����Ż¼ąĪŠÄų„ę¬Å─ĻPė┌╚▄ę║ų¬ūRĄ─ųžļy³cų¬ūR▀MąąĘų╬÷Ż¼ŽŻ═¹─▄Įo┤¾╝ęę╗ą®Ä═ų·�ĪŻ
ę╗��Īóņ`╗Ņæ¬ė├╚▄ĮŌČ╚Ė┼─Ņų¬ūRĮŌŅ}
ĪŠ└²1Ī┐į┌t1ĪµĢrŻ¼20┐╦╦«ųąūŅČÓ─▄╚▄ĮŌ15┐╦X�Ż¼t2ĪµĢr50┐╦╦«ųąūŅČÓ─▄╚▄ĮŌ30┐╦Y╬’┘|���ĪŻätX║═Yā╔ĘN╬’┘|Ą─╚▄ĮŌČ╚Ą─ĻPŽĄ╩Ū
A.X>Y B.X
ĪŠĮŌ╬÷Ī┐
ę└Ņ}ęŌų¬:▒ŠŅ}ī”╚▄ĮŌČ╚Ą─Ė┼─Ņ▀Mąą┴╦┴Ēę╗ĘN▌^×ķ│ķŽ¾Ą─└ĒĮŌ,╝┤į┌ę╗Č©┴┐Ą─╚▄ä®ųąūŅČÓ╚▄ĮŌ─│╬’┘|Ą─┘|┴┐,šf├„įō╚▄ę║ęčĮø▀_ĄĮ’¢║═.░┤šš╚▄ĮŌČ╚Ą─Č©┴xėŗ╦Ń:X╬’┘|Ą─╚▄ĮŌČ╚æ¬×ķ:15┐╦/20┐╦×100┐╦==75┐╦;Y╬’┘|Ą─╚▄ĮŌČ╚æ¬×ķ:30┐╦/50┐╦×100┐╦==60┐╦.ųĄĄ├ūóęŌĄ─╩Ū╚ń╣¹▒ŠŅ}▓╗ī”╚▄ĮŌČ╚Ą─Č©┴x▀Mąą╔Ņīė┤╬Ą─└ĒĮŌ,╚▌ęūš`▀xA▀xĒŚ.ė╔ė┌X║═Yā╔╬’┘|╦∙ī”æ¬Ą─£žČ╚▓╗ŽÓ═¼,╣╩╚▄ĮŌČ╚╩Ū¤oĘ©▀Mąą▒╚▌^Ą─.╣╩▒ŠŅ}Ą─┤░Ė×ķ:D.
ĪŠ└²2Ī┐─│£žČ╚Ž┬�����Ż¼īóA╬’┘|(▓╗║¼ĮYŠ¦╦«)Ą─╦«╚▄ę║Ęų│╔Ą╚┘|┴┐Ą─2Ę▌ĪŻŽ“Ą┌ę╗Ę▌╝ė╚ļ9┐╦A╬’┘|��Ż¼│õĘųöć░Ķ�����Ż¼▀Ćėą1┐╦╣╠¾w▓╗─▄╚▄ĮŌ;īóĄ┌Č■Ę▌╚▄ę║š¶░lĄ¶40┐╦╦«���Ż¼▓ó╗ųÅ═ĄĮįŁ£žČ╚Ż¼╚▄ę║ŪĪ║├’¢║═(¤oA╬÷│÷)����Ż¼ätA╬’┘|į┌įō£žČ╚Ž┬Ą─╚▄ĮŌČ╚╩Ū
A.40┐╦ B.20┐╦ C.8┐╦ D.¤oĘ©ėŗ╦Ń
ĪŠĮŌ╬÷Ī┐
ė╔Ņ}ęŌĘų╬÷┐╔ų¬Ż║▒ŠŅ}║¼ėąā╔éĆļ[║¼Śl╝■Ż║(1)Ęų│╔ā╔Ą╚Ę▌Ą─╚▄ę║ųąš¶░lĄ¶40┐╦╦«Č╝ŪĪ║├─▄ą╬│╔’¢║═╚▄ę║(2)š¶░lĄ¶40┐╦╦«ŪĪ║├─▄╚▄ĮŌ9-1==8┐╦A╬’┘|��ĪŻę“┤╦įŁŅ}ęŌ┐╔ęį▐D╗»×ķŻ║─│£žČ╚Ž┬Ż¼8┐╦A╬’┘|(▓╗║¼ĮYŠ¦╦«)╚▄ĮŌį┌40┐╦╦«ųąŪĪ║├ą╬│╔’¢║═╚▄ę║Ż¼įćŪ¾A╬’┘|į┌įō£žČ╚Ž┬Ą─╚▄ĮŌČ╚�ĪŻ’@╚╗�����Ż¼Įø▀^Ņ}ęŌ▐D╗»║¾ĮoĮŌŅ}ĦüĒ┴╦║▄┤¾Ą─ĘĮ▒ŃĪŻų▒ĮėŪ¾│÷┤░Ė×ķŻ║8┐╦/40┐╦ ×100┐╦==20┐╦ĪŻ
╣╩▒ŠŅ}Ą─┤░Ė×ķŻ║B�ĪŻ
Č■�Īóņ`╗Ņæ¬ė├╚▄ę║ĮM│╔ų¬ūRĮŌŅ}
ĪŠ└²3Ī┐ę¬╩╣A┐╦┘|┴┐ĘųöĄ×ķ20%Ą─╩│¹}╚▄ę║ūā×ķ┘|┴┐ĘųöĄ×ķ10%Ą─╚▄ę║����Ż¼┐╔ęį▓╔ė├Ą─ĘĮĘ©╩Ū
A.╝ė╚ļ0.8A┐╦╦« B.╝ė╦«╩╣╚▄ę║Ą─┘|┴┐×ķ2A
C.š¶░l╦«Ż¼╬÷│÷0.1A┐╦╣╠æB╩│¹}
D.╝ė╚ļ2A┐╦┘|┴┐ĘųöĄ×ķ5%Ą─╩│¹}╚▄ę║
ĪŠĮŌ╬÷Ī┐
▒ŠŅ}╩Ū┐╝▓ķĻPė┌╚▄ę║ĮM│╔ų¬ūRĄ─ę╗Ą└ŠC║Žąį▌^ÅŖĄ─įćŅ}���ĪŻĮŌ┤▒ŠŅ}Ą─ĻPµIį┌ė┌│õĘų└ĒĮŌ║═æ¬ė├╚▄┘|┘|┴┐ĘųöĄĄ─Č©┴xĪŻ
ī”ė┌AŻ║╝ė╚ļ0.8A║¾╚▄ę║ųą╚▄┘|Ą─┘|┴┐ĘųöĄ×ķŻ║(A×20%)/(A+0.8A)==11.1%
ī”ė┌BŻ║╝ė╚ļ╦«║¾╚▄ę║ųą╚▄┘|Ą─┘|┴┐ĘųöĄ×ķŻ║ (A×20%)/2A==10%
ī”ė┌CŻ║š¶░l╦«���Ż¼╬÷│÷0.1A┐╦╣╠æB╩│¹}║¾╚▄┘|Ą─┘|┴┐ūā×ķįŁüĒĄ─ę╗░ļŻ¼Ą½╚▄ę║Ą─┘|┴┐ūā×ķA-0.1A==0.9A,╣╩╚▄ę║ųą╚▄┘|Ą─┘|┴┐ĘųöĄę╗Č©┤¾ė┌10%
ī”ė┌DŻ║╝ė╚ļ2A┐╦┘|┴┐ĘųöĄ×ķ5%Ą─╩│¹}╚▄ę║║¾╚▄┘|Ą─┘|┴┐ĘųöĄ×ķŻ║
(A×20%+2A×5%)/(A+2A)==10%
ŠC║Žęį╔ŽĘų╬÷Ą├Ż║┤░Ė×ķB���ĪóDĪŻ

╚²�����Īóņ`╗Ņ▀\ė├╚▄ĮŌČ╚Ė┼─Ņ
ĮŌøQĮYŠ¦å¢Ņ}Ą─ėŗ╦Ń
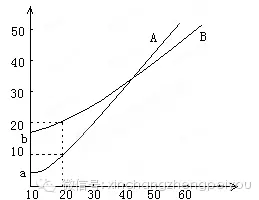
ĪŠ└²4Ī┐A�ĪóBā╔ĘN╗»║Ž╬’Ą─╚▄ĮŌČ╚Ū·ŠĆ╚ńłD╦∙╩ŠĪ�Ż¼Fę¬ė├ĮYŠ¦Ę©Å─A║═BĄ─╗ņ║Ž╬’ųą╠ß╚ĪA(▓╗┐╝æ]A��ĪóB╣▓┤µĢrī”Ė„ūį╚▄ĮŌČ╚Ą─ė░Ēæ)�����ĪŻ
(1)╚Ī50┐╦╗ņ║Ž╬’�Ż¼īó╦³╚▄ė┌100┐╦¤ß╦«Ż¼╚╗║¾└õģsĄĮ20ĪµĪŻ╚¶ę¬╩╣A╬÷│÷Č°B▓╗╬÷│÷����Ż¼ät╗ņ║Ž╬’ųąBĄ─┘|┴┐ĘųöĄ(B%)ūŅĖ▀▓╗─▄│¼▀^ČÓ╔┘?(īæ│÷═Ų└Ē╝░ėŗ╦Ń▀^│╠)
(2)╚ĪW┐╦╗ņ║Ž╬’�Ż¼īó╦³╚▄ė┌100┐╦¤ß╦«���Ż¼╚╗║¾└õģsĄĮ10Īµ���Ż¼╚¶╚į╚╗ę¬A╬÷│÷Č°B▓╗╬÷│÷���Ż¼šłīæ│÷į┌▀@ā╔ĘNŪķørŽ┬╗ņ║Ž╬’ųąAĄ─┘|┴┐ĘųöĄ(A%)æ¬įōØMūŃĄ─ĻPŽĄ╩Į(ęįW����Ż¼aŻ¼b▒Ē╩ŠŻ¼ų╗ąĶīó┤░Ė╠Ņį┌ÖMŠĆ╔Ž)
«öW
«öW>a+bĢr, A%
ĪŠĮŌ╬÷Ī┐
(1)į┌20ĪµĢr,╚¶ę¬╩╣B▓╗╬÷│÷,įō╚▄ę║ųąBĄ─┘|┴┐▓╗─▄│¼▀^20┐╦.ė╔ė┌A║═BĄ─┘|┴┐┐é║═×ķ50┐╦,╦∙ęį┤╦ĢrAĄ─┘|┴┐│¼▀^30┐╦,┤¾ė┌Ųõ╚▄ĮŌČ╚,A╬÷│÷,Ę¹║ŽŅ}ęŌ.
╝┤50┐╦×B%≤20┐╦,╝┤Ą├: B%≤40% ╗“ B%<40%.
(2)ę¬╩╣A╬÷│÷Č°B▓╗╬÷│÷,ų┴╔┘ę¬ØMūŃ:A%==a/(a+b),ę“×ķWa/W;
Č°«öW>a+bĢr,äta(W-b)/W.
╦─Īó╚▄ĮŌČ╚║═╚▄ę║ĮM│╔ų¬ūRĄ─ŠC║Žæ¬ė├
ĪŠ└²5Ī┐─│╬’┘|į┌20ĪµĢrĄ─╚▄ĮŌČ╚×ķ20┐╦����Ż¼į┌20Īµ Ģrīóįō╬’┘|20┐╦═Č╚ļ80┐╦╦«ųą│õĘų╚▄ĮŌ�Ż¼ätįō╬’┘|╚▄ę║ųą╚▄┘|Ą─┘|┴┐ĘųöĄ×ķ
A.25% B.20% C.16.7% D.¤oĘ©ėŗ╦Ń
ĪŠĮŌ╬÷Ī┐
▒ŠŅ}╩Ūę╗Ą└╚▄ĮŌČ╚║═╚▄┘|┘|┴┐ĘųöĄĄ─║åå╬ŠC║Žėŗ╦ŃŅ}�Ż¼ę▓╩Ūę╗Ą└╚▌ęūÕeĮŌĄ─įćŅ}ĪŻę└Ņ}ęŌų¬╩ūŽ╚▒žąĶę└ō■╚▄ĮŌČ╚ėŗ╦Ń│÷80┐╦╦«ųąūŅČÓ╚▄ĮŌ╚▄┘|Ą─┘|┴┐Ż║(įOūŅČÓ╚▄ĮŌĄ─┘|┴┐×ķX)ätėąX/80┐╦==20┐╦/100┐╦ X==16┐╦Ż¼╚╗║¾ę└ō■╚▄┘|Ą─┘|┴┐ĘųöĄĄ─Č©┴xėŗ╦ŃĄ├Ż║
16┐╦/(16┐╦+80┐╦)×100%==16.7%
╣╩┤░Ė×ķŻ║ CĪŻ
ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖC�����ĪóŲĮ░ÕĄ╚ęŲäėįOéõįLå¢ųą┐╝ŠW��Ż¼2024ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąą�ŻĪ>>³cō¶▓ķ┐┤














