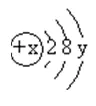┐╝³c1 įŁūėĄ─śŗ│╔
ó▒śŗ│╔įŁūėĄ─┴Żūė

ó▓į┌įŁūė└’Ż¼║╦ļŖ║╔öĄ=┘|ūėöĄ=║╦═ŌļŖūėöĄŻ¼įŁūė▓╗’@ļŖąįĪŻ
┐╝³c2 ŽÓī”įŁūė┘|┴┐
ó▒ŽÓī”įŁūė┘|┴┐Ą─ś╦£╩Ż║╠╝-12įŁūė┘|┴┐Ą─1/12ĪŻ
ó▓▒Ē▀_╩ĮŻ║Ar=Ųõ╦¹įŁūėĄ─┘|┴┐/(╠╝-12Ą─┘|┴┐×1/12)
ŽÓī”įŁūė┘|┴┐╩Ūę╗éĆ▒╚ųĄŻ¼▓╗╩ŪįŁūėĄ─īŹļH┘|┴┐ĪŻ
ó│įŁūėĄ─┘|┴┐ų„ę¬╝»ųąį┌įŁūė║╦╔ŽŻ¼ŽÓī”įŁūė┘|┴┐≈┘|ūėöĄ+ųąūėöĄ
┐╝³c3 į¬╦ž
ó▒į¬╦žĄ─Č©┴xŻ║Š▀ėąŽÓ═¼║╦ļŖ║╔öĄ(╝┤║╦ā╚┘|ūėöĄ)Ą─ę╗ŅÉįŁūėĄ─┐éĘQĪŻ
ó▓į¬╦žĄ─ĘNŅÉøQČ©ė┌║╦ļŖ║╔öĄ(╝┤║╦ā╚┘|ūėöĄ)ĪŻ
ó│ĄžÜżųą║¼┴┐┴ąŪ░╦─╬╗Ą─į¬╦ž(┘|┴┐ĘųöĄ)Ż║č§Īó╣ĶĪóõXĪóĶFŻ¼Ųõųą║¼┴┐ūŅČÓĄ─į¬╦ž(ĘŪĮī┘į¬╦ž)╩Ū觯¼║¼┴┐ūŅČÓĄ─Įī┘į¬╦ž╩ŪõXĪŻ
ó┤╔·╬’╝Ü░¹ųą║¼┴┐┴ąŪ░╦─╬╗Ą─į¬╦žŻ║č§Īó╠╝ĪóÜõĪóĄ¬ĪŻ
┐╝³c4 į¬╦žĘ¹╠¢
ó▒į¬╦žĘ¹╠¢Ż║ė├į¬╦žĄ─└ŁČĪ╬─├¹ĘQĄ─Ą┌ę╗éĆ┤¾īæūų─ĖüĒį¬╦žĪŻ
ó▓Ģ°īæŻ║
ó┼ė╔ę╗éĆūų─Ė▒Ē╩ŠĄ─į¬╦žĘ¹╠¢ę¬┤¾īæŻ¼╚ńŻ║HĪóOĪóSĪóCĪóPĄ╚ĪŻ
óŲė╔ā╔éĆūų─Ė▒Ē╩ŠĄ─į¬╦žĘ¹╠¢Ż¼Ą┌ę╗éĆūų─Ėę¬┤¾īæŻ¼Ą┌Č■éĆūų─ĖꬹĪīæ(╝┤“ę╗┤¾Č■ąĪ”)Ż¼╚ńŻ║CaĪóNaĪóMgĪóZnĄ╚ĪŻ
ó│į¬╦žĘ¹╠¢▒Ē╩ŠĄ─ęŌ┴xŻ║ó┼▒Ē╩Šę╗ĘNį¬╦ž;óŲ▒Ē╩Š▀@ĘNį¬╦žĄ─ę╗éĆįŁūėĪŻ└²╚ńŻ║
HŻ║ó┘▒Ē╩ŠÜõį¬╦ž
ó┌▒Ē╩Šę╗éĆÜõįŁūė
2HŻ║▒Ē╩ŠČ■éĆÜõįŁūėŻ¼2H▓╗─▄šf│╔Č■éĆÜõį¬╦ž
ūóęŌŻ║į¬╦žų╗ųvĘNŅÉŻ¼▓╗ųvéĆöĄ;įŁūė╝┤ųvĘNŅÉŻ¼ėųųvéĆöĄĪŻ
┐╝³c5 ╬’┘|ĮM│╔Īóśŗ│╔Ą─├Ķ╩÷
ó▒╬’┘|ė╔į¬╦žĮM│╔Ż║╚ń╦«╩Ūė╔Üõį¬╦ž║═č§į¬╦žĮM│╔Ą─ĪŻ
ó▓╬’┘|ė╔┴Żūė(ĘųūėĪóįŁūėĪóļxūė)śŗ│╔ĪŻ└²╚ńŻ║
ó┼╦«╩Ūė╔╦«Ęųūėśŗ│╔Ą─ĪŻ
óŲĮ╩Ūė╔ĮįŁūėśŗ│╔Ą─ĪŻ
óŪ┬╚╗»Ōc╩Ūė╔Ōcļxūė║═┬╚ļxūėśŗ│╔Ą─ĪŻ
ó│Ęųūė╩Ūė╔įŁūėśŗ│╔Ą─ĪŻ
╚ńŻ║╦«Ęųūė╩Ūė╔ÜõįŁūė║═č§įŁūėśŗ│╔Ą─;├┐éĆ╦«Ęųūė╩Ūė╔Č■éĆÜõįŁūė║═ę╗éĆč§įŁūėśŗ│╔Ą─ĪŻ
┐╝³c6 į¬╦žų▄Ų┌▒Ē║åĮķ
ó▒į¬╦žų▄Ų┌▒Ē

ó┼ų▄Ų┌▒Ē├┐ę╗ÖMąąĮąū÷ę╗éĆų▄Ų┌Ż¼╣▓ėą7éĆų▄Ų┌ĪŻ
óŲų▄Ų┌▒Ē├┐ę╗éĆ┐vąąĮąū÷ę╗ūÕŻ¼╣▓ėą16éĆūÕ(8Īó9Īó10╚²éĆ┐vąą╣▓═¼ĮM│╔ę╗éĆūÕ)ĪŻ
ó▓į¬╦žų▄Ų┌▒ĒĄ─ęŌ┴x
ó┼╩ŪīW┴Ģ║═蹊┐╗»īWų¬ūRĄ─ųžę¬╣żŠ▀;
óŲ×ķīżšęą┬į¬╦ž╠ß╣®┴╦└Ēšōę└ō■;
óŪė╔ė┌į┌į¬╦žų▄Ų┌▒Ēųą╬╗ų├įĮ┐┐Į³Ą─į¬╦žŻ¼ąį┘|įĮŽÓ╦ŲŻ¼┐╔ęįåó░l╚╦éāį┌į¬╦žų▄Ų┌▒ĒĄ─ę╗Č©ģ^ė“īżšęą┬╬’┘|(╚ń▐r╦ÄĪó┤▀╗»ä®Īó░ļī¦¾w▓─┴ŽĄ╚)ĪŻ
┐╝³c7 ║╦═ŌļŖūėĄ─Ęųīė┼┼▓╝
ó▒ļŖūė┼┼▓╝——Ęųīė┼┼▓╝Ż║Ą┌ę╗īė▓╗│¼▀^2éĆ;Ą┌Č■īė▓╗│¼▀^8éĆ;……ūŅ═Ōīė▓╗│¼▀^8éĆĪŻ
ó▓įŁūėĮYśŗ╩ŠęŌłDŻ║
ó┼║¼┴xŻ║(ęįµVįŁūėĮYśŗ╩ŠęŌłD×ķ└²)
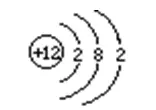
óŲįŁūėĄ─ūŅ═ŌīėļŖūėöĄ┼cį¬╦žĄ─ĘųŅÉĪó╗»īWąį┘|Ą─ĻPŽĄ

ó┘į¬╦žĄ─╗»īWąį┘|øQČ©ė┌įŁūėĄ─ūŅ═ŌīėļŖūėöĄĪŻ
ó┌įŁūėūŅ═ŌīėļŖūėöĄ×ķ8(║ż×ķ2)Ą─ĮYśŗĘQ×ķĘĆČ©ĮYśŗĪŻ
óŪįŁūėĪóĻ¢ļxūėĪóĻÄļxūėĄ─┼ąöÓ
ó┘ įŁūėŻ║┘|ūėöĄ=║╦═ŌļŖūėöĄ
ó┌ ĻÄļxūėŻ║┘|ūėöĄ<║╦═ŌļŖūėöĄ
ó█ Ļ¢ļxūėŻ║┘|ūėöĄ>║╦═ŌļŖūėöĄ
┐╝³c8 ļxūė
ó▒Č©┴xŻ║ĦļŖ║╔Ą─įŁūė(╗“įŁūėłF)ĪŻ
ó▓ĘųŅÉ(ūóŻ║▒Š╬─ųą╝ė£pŠ∙×ķ╔Žś╦)
Ļ¢ļxūėŻ║Ħš²ļŖ║╔Ą─ļxūėŻ¼╚ńNa+ĪóMg2+
ĻÄļxūėŻ║ĦžōļŖ║╔Ą─ļxūėŻ¼╚ńCl-ĪóO2-
ó│ļxūėĘ¹╠¢▒Ē╩ŠĄ─ęŌ┴xŻ║▒Ē╩Šļxūė(╗“ę╗éĆļxūė)Ż¼╚ńŻ║Mg2+——▒Ē╩ŠµVļxūė(ę╗éƵVļxūė)
2Mg2+ ——Ą┌ę╗éĆ2▒Ē╩Šā╔éƵVļxūė
Ą┌Č■éĆ2▒Ē╩Š├┐éƵVļxūėĦā╔éĆå╬╬╗Ą─š²ļŖ║╔
ó┼ļxūėĘ¹╠¢Ū░├µĄ─╗»īWėŗ┴┐öĄ(ŽĄöĄ)▒Ē╩ŠļxūėĄ─éĆöĄ;
óŲļxūėĘ¹╠¢Ą─▒Ē╩ŠĘĮĘ©Ż║į┌į¬╦žĘ¹╠¢(╗“įŁūėłF)ėę╔ŽĮŪ▒Ē├„ļxūė╦∙ĦĄ─ļŖ║╔Ż¼öĄųĄį┌Ū░Ż¼š²Īóžō╠¢į┌║¾ĪŻļxūėĦ1éĆå╬╬╗Ą─š²ļŖ║╔╗“éĆå╬╬╗Ą─žōļŖ║╔Ż¼“1”╩Ī┬į▓╗īæĪŻ╚ńŻ║ Ļ¢ļxūėŻ║Na+ĪóCa2+ĪóAl3+Ą╚Ż¼ĻÄļxūėŻ║Cl-ĪóS2‑Ą╚
ó┤ėąĻPļxūėĄ─ąĪĮY
ó┼Įī┘ļxūėĦš²ļŖ║╔Ż¼ĘŪĮī┘ļxūėĦžōļŖ║╔;
óŲļxūė╦∙ĦĄ─ļŖ║╔=įōį¬╦žĄ─╗»║Žār
óŪ│ŻęŖįŁūėłFļxūė(šłūóęŌ╔ŽŽ┬ś╦)
SO42- ┴“╦ßĖ∙ļxūė CO32- ╠╝╦ßĖ∙ļxūė
NO3- Ž§╦ßĖ∙ļxūė OH- Üõč§Ė∙ļxūė
NH4+ õ@Ė∙ļxūė
┐╝³c9 ╗»īW╩Į
ó▒╗»īW╩ĮĄ─īæĘ©
A.å╬┘|Ą─╗»īW╩Į
ó┼ļpįŁūėĘųūėĄ─╗»īW╩ĮŻ¼╚ńŻ║ÜõÜŌ——H2Ż¼č§ÜŌ——O2Ż¼Ą¬ÜŌ——N2Ż¼┬╚ÜŌ——Cl2ĪŻ
óŲŽĪėąÜŌ¾wĪóĮī┘┼c╣╠¾wĘŪĮī┘å╬┘|Ż║ė╔įŁūėśŗ│╔Ż¼╦³éāĄ─╗»īW╩Įė├į¬╦žĘ¹╠¢üĒ▒Ē╩ŠĪŻ
B.╗»║Ž╬’Ą─╗»īW╩Į
š²ārīæū¾▀ģŻ¼žōārīæėę▀ģŻ¼═¼Ģrš²Īóžō╗»║ŽārĄ─┤·öĄ║═×ķ┴ŃĪŻ
ó▓Äū³cūóęŌ╩┬ĒŚ
ó┼ę╗ĘN╬’┘|ų╗ėąę╗éĆ╗»īW╩ĮŻ¼Ģ°īæ╗»īW╩ĮĢrŻ¼ę¬┐╝æ]ĄĮį¬╦žĄ─┼┼┴ąĒśą“Ż¼▀Ćę¬┐╝æ]ĄĮ▒Ē╩ŠįŁūėéĆöĄĄ─ĮŪ┤aæ¬īæĄ─▓┐╬╗ĪŻ
óŲę╗░Ń╗»║Ž╬’Ą─ųą╬─├¹ĘQŻ¼ŲõĒśą“║═╗»īW╩ĮĢ°īæĄ─Ēśą“š²║├ŽÓĘ┤ĪŻ
ó│╗»īW╩ĮĄ─║Ł┴x(ęįCO2×ķ└²šf├„)
ó┼║Ļė^╔Ž
▒Ē╩Šę╗ĘN╬’┘|Ż║▒Ē╩ŠČ■č§╗»╠╝ĪŻ
▒Ē╩Šįō╬’┘|ė╔──ą®į¬╦žĮM│╔Ż║▒Ē╩ŠČ■č§╗»╠╝ė╔╠╝į¬╦ž║═č§į¬╦žĮM│╔ĪŻ
óŲ╬óė^╔Ž
▒Ē╩Šįō╬’┘|Ą─ę╗éĆĘųūėŻ║▒Ē╩Šę╗éĆČ■č§╗»╠╝ĘųūėĪŻ
▒Ē╩ŠĘųūėĄ─śŗ│╔Ż║▒Ē╩Š├┐éĆČ■č§╗»╠╝Ęųūėė╔ę╗éĆ╠╝įŁūė║═Č■éĆč§įŁūėśŗ│╔ĪŻ
┐╝³c10 ╗»║Žār
ó▒į¬╦ž╗»║ŽārĄ─▒Ē╩ŠĘĮĘ©
╗»║Žārė├+1Īó+2Īó+3Īó-1Īó-2……▒Ē╩ŠŻ¼ś╦į┌į¬╦žĘ¹╠¢Ą─š²╔ŽĘĮŻ¼╚ńŻ║NaĪó ClĪó MgĪó OĪŻę¬ūóęŌ╗»║ŽārĄ─▒Ē╩ŠĘĮĘ©┼cļxūėĘ¹╠¢Ą─ģ^äeŻ¼ļxūė╦∙ĦļŖ║╔Ę¹╠¢ė├+Īó2+Īó-Īó2-……▒Ē╩ŠŻ¼ś╦į┌į¬╦žĘ¹╠¢Ą─ėę╔ŽĮŪŻ¼╚ńŻ║
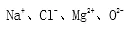
ó▓į¬╦ž╗»║ŽārĄ─ę╗░ŃęÄ┬╔
ó┼Üõį¬╦žĄ─╗»║Žār═©│Ż’@+1ārŻ¼č§į¬╦žĄ─╗»║Žār’@-2ārĪŻ
óŲį┌╗»║Ž╬’ųąŻ¼Įī┘į¬╦ž×ķš²ārĪŻ
óŪĘŪĮī┘┼cÜõ╗“Įī┘╗»║ŽĢrŻ¼ĘŪĮī┘į¬╦ž’@žōār;ĘŪĮī┘┼cč§į¬╦ž╗»║ŽĢrŻ¼ĘŪĮī┘į¬╦ž’@š²ārĪŻ
ó╚į┌╗»║Ž╬’ųąŻ¼š²Īóžō╗»║ŽārĄ─┤·öĄ║═×ķ┴ŃĪŻ
ó╔į┌å╬┘|ųąį¬╦žĄ─╗»║Žār×ķ┴ŃĪŻ
ó│└╬ėø│ŻęŖį¬╦žĄ─╗»║Žār
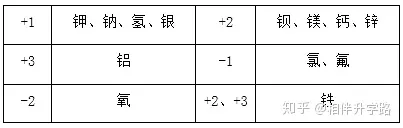
ó┤│ŻęŖĖ∙(įŁūėłF)Ą─╗»║Žār
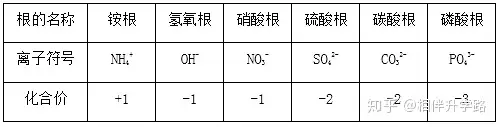
│ŻęŖį¬╦žĄ─╗»║Žār(š²ār)Ż║
ę╗ārŌøŌcÜõ┼cŃyŻ¼Č■ārŌ}µVõ^┼cõ\Ż¼╚²ārĮī┘į¬╦žõX;
ę╗╬ÕŲ▀ūāār┬╚Ż¼Č■╦─╬ÕĄ¬Ż¼┴“╦─┴∙Ż¼╚²╬Õėą┴ūŻ¼Č■╦─╠╝;
ę╗Č■Ń~Ż¼Č■╚²ĶFŻ¼Č■╦─┴∙Ų▀Õi╠žäeĪŻ
óĄ╗»║ŽārĄ─æ¬ė├
ó┼Öz“×╗»īW╩ĮĄ─š²š`;
óŲĖ∙ō■╗»īW╩Į┼ąöÓį¬╦žĄ─╗»║Žār;
óŪĖ∙ō■į¬╦žĄ─╗»║Žār═ŲŪ¾īŹļH┤µį┌╬’┘|Ą─╗»īW╩ĮĪŻ
┐╝³c11 ėąĻP╗»īW╩ĮĄ─ėŗ╦Ń
ó▒ėŗ╦Ń╬’┘|Ą─ŽÓī”Ęųūė┘|┴┐=Ė„į¬╦žĄ─ŽÓī”įŁūė┘|┴┐×įŁūėéĆöĄų«║═
ó▓ėŗ╦Ń╬’┘|ĮM│╔į¬╦žĄ─┘|┴┐▒╚=Ė„į¬╦žĄ─ŽÓī”įŁūė┘|┴┐×įŁūėéĆöĄų«▒╚
ó│ėŗ╦Ń╬’┘|ųą─│į¬╦žĄ─┘|┴┐ĘųöĄ
╬’┘|ųą─│į¬╦žĄ─┘|┴┐ĘųöĄ=(įōį¬╦žĄ─ŽÓī”įŁūė┘|┴┐×įŁūėéĆöĄ)÷╗»║Ž╬’Ą─ŽÓī”Ęųūė┘|┴┐×100%
ó┤ėŗ╦Ńę╗Č©┘|┴┐Ą─╗»║Ž╬’ųą║¼─│į¬╦žĄ─┘|┴┐
─│į¬╦žĄ─┘|┴┐=╗»║Ž╬’Ą─┘|┴┐×╗»║Ž╬’ųąįōį¬╦žĄ─┘|┴┐ĘųöĄ
ūāą╬Ż║╗»║Ž╬’Ą─┘|┴┐=─│į¬╦žĄ─┘|┴┐÷╗»║Ž╬’ųąįōį¬╦žĄ─┘|┴┐ĘųöĄ
óĄęčų¬╗»║Ž╬’ųąĖ„į¬╦žĄ─┘|┴┐▒╚║═Ė„į¬╦žĄ─ŽÓī”įŁūė┘|┴┐Ż¼Ū¾įŁūėéĆöĄ▒╚
Ė„į¬╦žĄ─įŁūėéĆöĄ▒╚=Ė„į¬╦žĄ─┘|┴┐/Ė„į¬╦žĄ─ŽÓī”įŁūė┘|┴┐ų«▒╚
Öz£yŅ}
ę╗Īó▀xō±Ņ}(▒ŠŅ}╣▓10ąĪŅ}Ż¼├┐ąĪŅ}ų╗ėąę╗éĆ▀xĒŚĘ¹║ŽŅ}ęŌĪŻ├┐ąĪŅ}2ĘųŻ¼╣▓20Ęų)
1.į┌Ąžš║¾Ą─Š╚į«ąąäėųąŻ¼×ķ┴╦╦č╦„┬±į┌ÅUąµųąĄ─ąę┤µš▀Ż¼╚╦éāė├┴╦╦čŠ╚╚«Ż¼╦čŠ╚╚«─▄Ė∙ō■╚╦¾w░l│÷Ą─ÜŌ╬Č░l¼Fąę┤µš▀ĪŻįćė├╗»īWė^³cÅ─╬ó┴ŻĄ─ĮŪČ╚Ęų╬÷─▄░l¼Fąę┤µš▀Ą─įŁę“╩Ū( )
A.Ęųūėį┌▓╗öÓ▀\äė B.ĘųūėķgėąķgĖ¶
C.ĘųūėĄ─¾wĘe║▄ąĪ D.ĘųūėĄ─┘|┴┐║▄ąĪ
2.Ž┬┴ą▀xĒŚųą┤·▒ĒļxūėĄ─╩Ū(šf├„Ż║öĄūų┤·▒Ē┘|ūėöĄŻ¼“+”▒Ē╩ŠįŁūė║╦╦∙ĦĄ─ļŖ║╔Ż¼║┌³c┤·▒Ē║╦═ŌļŖūė) ( )
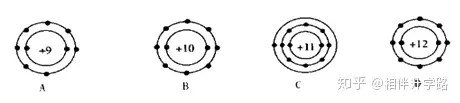
3.Ęųūė║═įŁūėĄ─Ė∙▒Šģ^äe╩Ū( )
A.Ęųūė▒╚įŁūė┤¾
B.Ęųūė┐╔ĘųŻ¼įŁūė▓╗┐╔Ęų
C.į┌╗»īWūā╗»ųąŻ¼Ęųūė┐╔ęįį┘ĘųŻ¼įŁūė▓╗─▄į┘Ęų
D.Ęųūė┐╔ęįśŗ│╔╬’┘|Ż¼įŁūė▓╗─▄śŗ│╔╬’┘|
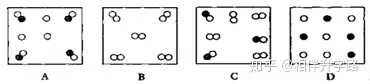
4.Ž┬┴ąĖ„ĮMįŁūėĮYśŗ╩ŠęŌłDųąŻ¼╦∙▒Ē╩ŠĄ─ā╔ĘNį¬╦žŠ▀ėąŽÓ╦Ų╗»īWąį┘|Ą─╩Ū ( )
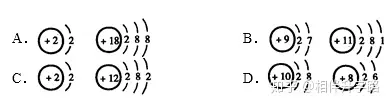
5.─▄ūC├„Ęųūėį┌╗»īWĘ┤æ¬ųą┐╔ęįį┘ĘųĄ─╩┬īŹ╩Ū( )
A.č§╗»╣» ╩▄¤ßĘųĮŌ B.ė├ūįüĒ╦«ųŲš¶s╦«
C.Ęųļx┐šÜŌĘ©ųŲč§ÜŌ D.ĄŌ╔²╚A×ķĄŌš¶ÜŌ
6.Ž┬┴ą▓┘ū„─▄īó╬’┘|═Ļ╚½Ęų╔ó│╔ ĘųūėĄ─╩ŪBC╬┤īWĄĮ ( )
A.į┌čą└Å└’ė├ĶŲčą─ź┴ŻĀŅ─æĄ\ B.īóšß╠Ū╚▄ė┌╦«
C.░čų▓╬’ė═Ą╬╚ļ╦«ųąė├┴”š±╩Ä D.╝ė¤ßĖ▀Õi╦ßŌø
7.AĪóBĪóC╚²ų╗ąĪ¤²▒Łā╚ę└┤╬╩óėąę╗Č©¾wĘeĄ─ØŌ░▒╦«ĪóĘė╠¬╚▄ę║ĪóĘė╠¬╚▄ę║Ż¼░┤łD╦∙╩Š▀Mąą╠ĮŠ┐╗ŅäėŻ¼▓╗─▄Ą├ĄĮĄ─ĮYšō╩Ū( )
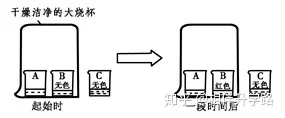
A. ░▒Ęųūė╩Ū▓╗öÓ▀\äėĄ─
B. ēA─▄╩╣Ęė╠¬╚▄ę║ūā╝t
C. ┐šÜŌ▓╗─▄╩╣Ęė╠¬╚▄ę║ūā╝t
D.░▒Ęųūė╚▄ė┌╦«Ż¼ą╬│╔░▒╦«╩╣Ęė╠¬╚▄ę║ūā╝t
8.Ž┬┴ąī”╔·«aĪó╔·╗Ņ¼FŽ¾Ą─ĮŌßīš²┤_Ą─╩Ū( )
A.õXÕVļy▒╗ē║┐sŻ¼ę“×ķõXįŁūėķgø]ėąķgŽČ
B.£žČ╚ėŗ└’Ą─╣»ų∙Ž┬ĮĄŻ¼ę“×ķįŁūėļS£žČ╚Ą─ĮĄĄ═Č°ūāąĪ
C.╩»ė═ÜŌ╝ėē║║¾┘A┤µį┌õōŲ┐ųąŻ¼ę“×ķÜŌ¾wĘųūė¾wĘe║▄ąĪ
D.č§ÜŌ║═ę║č§Č╝┐╔ęįų·╚╝Ż¼ę“×ķŽÓ═¼╬’┘|Ą─ĘųūėŻ¼Ųõ╗»īWąį┘|ŽÓ═¼
9.─│ą®╗©ŹÅÄr╩»▓─ųą║¼ėąĘ┼╔õąįį¬╦žļ▒Ż¼ę╗ĘNļ▒įŁūėĄ─┘|ūėöĄ×ķ86Ż¼ųąūėöĄ×ķ136Ż¼▀@ĘNļ▒įŁūėĄ─║╦═ŌļŖūėöĄ×ķ( )
A.50 B.86
C.136 D.222
10.į¬╦žų▄Ų┌▒Ē╩ŪīW┴Ģ╗»īWĄ─ųžę¬╣żŠ▀ĪŻėęłD╩Ūį¬╦žų▄Ų┌▒ĒųąĄ─ę╗Ė±Ż¼Å─ųą½@╚ĪĄ─ą┼ŽóÕeš`Ą─╩Ū( )
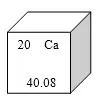
A.įōį¬╦žĄ─įŁūėą“öĄ×ķ20
B.įōį¬╦žī┘ė┌ĘŪĮī┘į¬╦ž
C.įōį¬╦žĄ─įŁūė║╦═Ōėą20éĆļŖūė
D.įōį¬╦žĄ─ŽÓī”įŁūė┘|┴┐×ķ40.08
Č■Īó▀xō±Ņ}(▒ŠŅ}╣▓5ąĪŅ}Ż¼├┐ąĪŅ}ėąę╗éĆ╗“ā╔éĆ▀xĒŚĘ¹║ŽŅ}ęŌĪŻÕe▀xĪóČÓ▀x▓╗ĮoĘųĪŻėąā╔éĆ┤░ĖĄ─Ż¼ų╗▀xę╗éĆŪęš²┤_Ż¼Įo2ĘųĪŻ├┐ąĪŅ}3ĘųŻ¼╣▓15Ęų)
11.╩«Š┼╩└╝o│§Ż¼ęŌ┤¾└¹┐ŲīW╝ę░óĘ³╝ėĄ┬┴_į┌┐éĮYŪ░╚╦╣żū„Ą─╗∙ĄA╔ŽŻ¼╠ß│÷┴╦ĘųūėĄ─Ė┼─ŅŻ¼╦¹šJ×ķŻ║ó┘ę╗Ūą╬’┘|Č╝╩Ūė╔Ęųūėśŗ│╔Ą─;ó┌Ęųūėė╔įŁūėśŗ│╔;ó█įŁūė▓╗─▄¬Ü┴ó┤µį┌;ó▄Ęųūė╩Ū▒Ż│ų╬’┘|╗»īWąį┘|Ą─ūŅąĪ┴Żūė;ó▌ĘųūėĄ─┘|┴┐Ą╚ė┌ĮM│╔╦³Ą─įŁūėĄ─┘|┴┐ų«║═;ó▐Ęųūėį┌▓╗═ŻĄž▀\äėĪŻÅ──Ń╦∙īWĄ─ų¬ūR┐┤Ż¼╔Ž╩÷ė^³c┤µį┌├„’@▓╗ūŃĄ─╩Ū ( )
A.ó┘ó█ B.ó┘ó┌ó▌
C.ó▄ó▌ó▐ D.ó█ó▌
12.Ž┬┴ąĻPė┌FeĪóFe2+ĪóFe3+Ą─šfĘ©ųąŻ¼š²┤_Ą─╩Ū( )
A.╦³éāĄ─┘|ūėöĄ▓╗═¼
B.╦³éāĄ─ūŅ═ŌīėļŖūėöĄŽÓ═¼
C.╦³éāĄ─║╦═ŌļŖūėöĄ▓╗═¼
D.╦³éāī┘ė┌═¼ę╗ĘNį¬╦ž
13.Ž┬łD╩ŪÜŌ¾w╬’┘|Ą─┴Żūė╩ŠęŌłDŻ¼łDųą“ ”║═“ ”Ęųäe▒Ē╩Šā╔ĘN▓╗═¼Ą─įŁūėŻ¼Ųõųą▒Ē╩Š╝āā¶╬’Ą─╩Ū( )
14.╗»īW╔Ž│Żė├į¬╦žĘ¹╠¢ū¾Ž┬ĮŪĄ─öĄūų▒Ē╩ŠįŁūėĄ─┘|ūėöĄŻ¼ū¾╔ŽĮŪĄ─öĄūų▒Ē╩ŠįŁūėĄ─ųąūėöĄ┼c┘|ūėöĄų«║═Ż¼╚ńė├ C▒Ē╩Š║╦ā╚ėą6éĆ┘|ūė║═7éĆųąūėĄ─╠╝įŁūėĪŻät Cl║═ Cl( )
A.įŁūė║╦ā╚┘|ūėöĄ─┐▓╗═¼
B.ī┘ė┌═¼ĘNį¬╦ž
C.įŁūėųą║╦═ŌļŖūėöĄŽÓ═¼
D.įŁūė║╦ā╚ųąūėöĄ─┐ŽÓ═¼
15.ā╔╬╗├└ć°┐ŲīW╝ę▒╦Ą├·░óĖ±└ū║═┴_Ą├└’┐╦·¹£Į▐rŻ¼ę“×ķ░l¼F╝Ü░¹─ż╦«═©Ą└Ż¼ęį╝░ī”ļxūė═©Ą└ĮYśŗ║═ÖC└Ē蹊┐ū„│÷Ą─ķ_äōąįžĢ½IČ°½@Ą├2003─ĻųZžÉĀ¢╗»īW¬äĪŻ╦¹éāų«╦∙ęį½@Ą├ųZžÉĀ¢╗»īW¬äČ°▓╗╩Ū╔·└ĒīW╗“ßtīW¬ä╩Ū( )
A.╦¹éāĄ─蹊┐║═╗»īW╬’┘|╦«ėąĻP
B.╦¹éāĄ─蹊┐ėą└¹ė┌čąųŲßśī”ę╗ą® ╔±ĮøŽĄĮy╝▓▓Ī║═ą─č¬╣▄╝▓▓ĪĄ─╦Ä
C.╦¹éāĄ─蹊┐╔Ņ╚ļĄĮĘųūėĪóįŁūėĄ─īė┤╬
D.╦¹éāĄ─蹊┐╔Ņ╚ļĄĮ╝Ü░¹Ą─īė┤╬
╚²Īó╠Ņ┐šŅ}(▒ŠŅ}░³└©10ąĪŅ}ĪŻ(17Īó21Īó25├┐┐š2ĘųŻ¼ŲõėÓ├┐┐š1ĘųŻ¼╣▓65Ęų)
16.(5Ęų)═©▀^īW┴Ģ╬ęéāī”“╬’┘|śŗ│╔Ą─ŖW├ž ”ęčėąę╗Č©Ą─┴╦ĮŌĪŻšłį┌ėęłDĘĮ┐“ųą╠Ņīæ┴Żūė├¹ĘQŻ¼▒Ē╩ŠĖ„ĘN┴Żūė╩Ūį§śėśŗ│╔╬’┘|Ą─ĪŻ
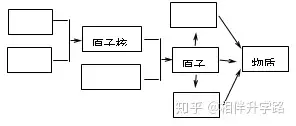
17.(6Ęų)ė├ĘųūėįŁūėĄ─ė^³cĮŌßīŽ┬┴ą¼FŽ¾Ż║
(1)رę┬Ę■┴└į┌╠½Ļ¢Ģ±ų°Ą─ĄžĘĮĖ³╚▌ęūĖ╔ĪŻ
(2)1LŠŲŠ½║═1L╦«╗ņ║ŽŻ¼┐é¾wĘeąĪė┌2LĪŻ
(3)£žČ╚ėŗ└’Ą─╦«Ńy╩▄¤ß¾wĘe┼“├øĪŻ
18.(8Ęų)░┤ę¬Ū¾īæ│÷Ž┬┴ą╬’┘|Ą─╗»īW╩Į(Ė„īæ2éĆ)Ż║
(1)ė╔Ęųūėśŗ│╔Ą─╬’┘| _____;
(2)ė╔įŁūėų▒Įėśŗ│╔Ą─╬’┘|_____;
(3)ė╔ļxūėśŗ│╔Ą─╬’┘|______ ;
(4)═¼ĘNį¬╦žĮM│╔Ą─▓╗═¼╬’┘|_____;
19.(6Ęų)į┌ó┘ĘųūėĪóó┌įŁūėĪóó█┘|ūėĪóó▄ųąūėĪóó▌ļŖūėĪóó▐ļxūė▀@ą®╬ó┴ŻųąŻ║
(1)─▄śŗ│╔╬’┘|Ą─╬ó┴Żėą__________;
(2)’@ļŖųąąįĄ─╬ó┴Żėą______ ______;
(3)┘|┴┐ūŅąĪĄ─╬ó┴Ż╩Ū____________;
(4)ę╗ȩĦš²ļŖ║╔Ą─╬ó┴Żėą____ ______;
(5)ę╗ȩĦžōļŖĄ─╬ó┴Żėą__________;
(6)┐╔─▄Ħš²ļŖę▓┐╔─▄ĦžōļŖĄ─╩Ū_____ ĪŻ
20.(10Ęų)ėęłD╩Ū─│┴ŻūėĄ─ĮYśŗ╩ŠęŌłDŻ¼╗ž┤Ž┬┴ąå¢Ņ}Ż║
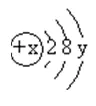
(1)x▒Ē╩Š_____Ż¼╦³øQČ©į¬╦žĄ─_____Ż¼y▒Ē╩Š_____ Ż¼╦³øQČ©į¬╦žĄ─_____Ż¼įōį¬╦ž╬╗ė┌į¬╦žų▄Ų┌▒ĒĄ┌_____ų▄Ų┌ĪŻ
(2)«öx=12ĢrŻ¼y=_____Ż¼įō┴Żūė×ķįŁūėĪŻ
(3)«öx=17ĢrŻ¼įō┴ŻūėĦ1éĆå╬╬╗žōļŖ║╔Ż¼äty=___ĪŻ
(4)«öy=1ĢrŻ¼įō┴Żūėęū_______ļŖūėŻ¼ūā│╔Ħ_____ļŖ║╔Ą─_________ĪŻ
21.(6Ęų)ėęłD×ķč§╗»╣»╩▄¤ßĘųĮŌĄ─╬óė^▀^│╠╩ŠęŌłDĪŻ
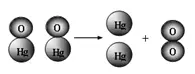
Å─łD╩Šųą─▄┐éĮY│÷──ą®ęÄ┬╔(ų┴╔┘īæ3Śl)Ż║
(1)_________________ĪŻ
(2)_________________ĪŻ
(3)_________________ĪŻ
22.(5Ęų)2011─Ļ3į┬11╚šŽ┬╬ńŻ¼╚š▒Šīm│Ū┐h░l╔·└’╩Ž9.0╝ē┤¾ĄžšŻ¼ę²░lĄ─║Żć[ī¦ų┬ĖŻŹu║╦ļŖšŠ░l╔·ųž┤¾║╦╩┬╣╩ĪŻ
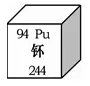
(1)║╦ļŖšŠųą║╦╚╝┴ŽŌÖ╗“Ņąį┌ųąūėĄ─ū▓ō¶Ž┬Ż¼įŁūė║╦░l╔·Ęų┴čŻ¼«a╔·õ^Īóļ»ĪóĄŌĪóõCĪóµJĄ╚įŁūė║═ę╗ą®┴Żūė╝░╔õŠĆŻ¼═¼ĢrßīĘ┼┤¾┴┐Ą──▄┴┐Ż¼▀@ą®─▄┴┐┐╔ė├ė┌“īäėŲ¹▌åÖC░lļŖĪŻ
ó┘Å─╬’┘|Ą─ūā╗»╔Ž┐┤Ż¼║╦ūā╗»┼c╗»īWūā╗»Ą─ŽÓ═¼³c╩Ū _____;Å─įŁūėĄ─ūā╗»╔Ž┐┤Ż¼║╦ūā╗»┼c╗»īWūā╗»Ą─▓╗═¼³c╩Ū_____ĪŻ
ó┌ėęłD×ķį¬╦žų▄Ų┌▒ĒųąŅąį¬╦žĄ─ŽÓĻPą┼ŽóŻ¼Ž┬┴ąšfĘ©š²┤_Ą─╩Ū_____ĪŻ
A.Ņą╩ŪĮī┘į¬╦ž B.ŅąįŁūė║╦═Ōėą94éĆļŖūė
C.Ņąį¬╦žĄ─ųąūėöĄ94 D.ŅąĄ─ŽÓī”įŁūė┘|┴┐×ķ244g
(2)ßśī”╚š▒Š║╦ą╣┬®╩┬╣╩Įo╚╦ŅÉĦüĒĄ─×─ļyŻ¼ėą═¼īW╠ß│÷╚ńŽ┬┐┤Ę©Ż║“┐ŲīW╝╝ągĮo╚╦ŅÉ▀M▓ĮĦüĒ┴╦žĢ½IŻ¼ę▓ĦüĒ┴╦×─ļyŻ¼┐╔ęŖŻ¼┐ŲīW╝╝ągī”╚╦ŅÉ░lš╣▓óø]ėą╠½┤¾ęŌ┴xĪŻ”─Ń╩Ūʱ═¼ęŌ┤╦┐┤Ę©Ż¼šłšäšä─ŃĄ─ė^³cĪŻ
23.(6Ęų)įćę└ō■║╦ļŖ║╔öĄ×ķ1Ī½18Ą─į¬╦žĄ─įŁūėĮYśŗ╩ŠęŌłDŻ¼╗ž┤Ž┬┴ąå¢Ņ}Ż║
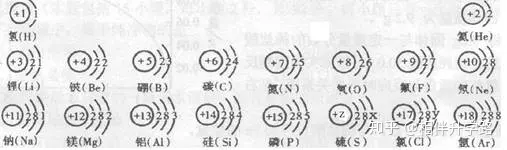
(1)╔ŽłDųą┴“į¬╦žĄ─║╦ļŖ║╔öĄz=_______;┬╚į¬╦žĄ─ūŅ═ŌīėļŖūėöĄy=______(╠ŅöĄųĄ)Ż¼ät┼c┬╚į¬╦ž╗» īWąį┘|ŽÓ╦ŲĄ─į¬╦ž╩Ū______ĪŻ
(2)║╦ļŖ║╔öĄ×ķ12Ą─į¬╦žĄ─įŁūė╩¦╚źā╔éĆļŖūė║¾Ż¼ą╬│╔Ą─┴ŻūėĄ─Ę¹╠¢╩Ū______Ż¼╦³Ą─║╦═ŌļŖūė┼┼▓╝┼c_______į¬╦žĄ─įŁūė║╦═ŌļŖūė┼┼▓╝ŽÓ═¼ĪŻ
(3)╔ŽłDĄ─┼┼┴ąŠ▀ėąę╗Č©Ą─ęÄ┬╔Ż¼╚ńŻ║═¼ę╗ąąųąŻ¼Å─ū¾ĄĮėęį¬╦žĄ─║╦ļŖ║╔öĄę└┤╬į÷╝ėĪŻ─Ń▀Ć─▄šęĄĮ──ą®ęÄ┬╔?įćīæ│÷Ųõųąę╗éĆŻ║
_________________________________________
24.(5Ęų)Ž┬łD╩Ū1Ī½18╠¢į¬╦žįŁūėūŅ═ŌīėļŖūėöĄ┼cįŁūė║╦ļŖ║╔öĄĄ─ĻPŽĄłDĪŻ
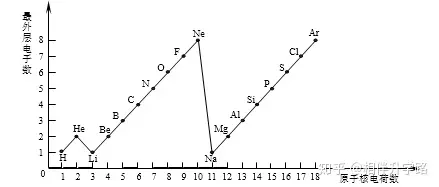
įć╗ž┤Ż║
(1)ę╗éĆ╦«Ęųūė╣▓ėą____éĆįŁūė║╦Īó____éĆ┘|ūėĪŻ
(2)ę╗éĆMg2+║╦═Ō╣▓ėą____éĆļŖūėŻ¼Cl—Ą─ūŅ═ŌīėļŖūėöĄ║═____įŁūėĄ─ūŅ═ŌīėļŖūėöĄŽÓ═¼ĪŻ
(3)═©▀^╔ŽłD─Ń─▄░l¼F──ą®ęÄ┬╔?šłīæ│÷Ųõųąę╗éĆŻ║
__________________________________ ĪŻ
25.(8Ęų)ėęŽ┬łD╩ŪÅ─┐šÜŌųąĘųļxč§ÜŌĄ─╩ŠęŌłDŻ║šł─Ńīæ│÷Å─łDųą╦∙½@Ą├Ą─ėąĻP╬’┘|ĮM│╔ĪóĮYśŗĪóąį┘|Īóūā╗»Ą╚ą┼ŽóĖ„ę╗ŚlŻ║
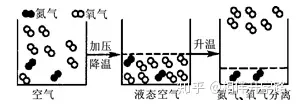
ĮM│╔Ż║_____________ĪŻ
ĮYśŗŻ║_____________ĪŻ
ąį┘|Ż║_____________ĪŻ
ūā╗»Ż║_____________ĪŻ

ĪĪĪĪ ÜgėŁ╩╣ė├╩ųÖCĪóŲĮ░ÕĄ╚ęŲäėįOéõįLå¢ųą┐╝ŠWŻ¼2024ųą┐╝ę╗┬Ę┼Ń░ķ═¼ąąŻĪ>>³cō¶▓ķ┐┤